新股消息 | 丹诺医药递表港交所 拥有利福特尼唑(TNP-2198)等三大核心产品
查投资获悉,据港交所7月30日披露,丹诺医药(苏州)股份有限公司(简称:丹诺医药)向港交所主板递交上市申请,中信证券和农银国际为联席保荐人。

招股书显示,丹诺医药于2013年注册成立,是一家临近商业化阶段的生物科技公司,专注于发现、开发及商业化差异化的创新药产品,以解决细菌感染及细菌代谢相关疾病领域的未被满足临床需求。凭借自主开发的多靶点偶联分子技术,公司致力于为患者提供最佳治疗方案,以克服传统治疗的局限性并改善患者预后。截至最后实际可行日期,公司已建立一条由七项创新资产组成的差异化管线,包括三项核心产品:即利福特尼唑(TNP-2198),是全球首个且唯一治疗幽门螺杆菌(“幽门螺杆菌”)感染的新分子实体(“NME”)候选药物;利福喹酮(TNP-2092)注射剂,一款潜在首创三靶点治疗植入体相关细菌感染的候选药物;及TNP-2092口服制剂,全球首个用于治疗肠道菌群代谢相关疾病的多靶点候选药物。
核心产品利福特尼唑(TNP-2198)是由利福霉素药效团和硝基咪唑药效团构建的稳定偶联药物。通过抑制RNA聚合酶和硝基还原酶激活产生高活性物质实现杀菌作用,对微需氧菌和厌氧菌具有协同双重作用机制。利用这种独特的多靶点机制,利福特尼唑有望克服抗菌药物耐药性这一重要且日益严重的全球挑战。作为三联疗法的一部分,与目前指南推荐的一线治疗方案铋剂四联疗法(“BQT”)相比,利福特尼唑在疗效、安全性、临床应用和患者潜在依从性方面具有显著优势。
丹诺医药已完成利福特尼唑三联疗法(“RTT”)对比BQT的中国III期头对头临床试验,并计划于2025年8月底前向国家药品监督管理局(“国家药监局”)提交新药上市申请(“NDA”)。临床试验结果表明,RTT在根除率、安全性及耐受性方面较BQT均有优势。值得注意的是,在多重耐药人群中,RTT显示出对BQT的优效性(89.9%vs.81.2%;差值:8.7%;非劣检验p<0.0001;优效检验p=0.023)。这项试验的结果显示,RTT组的临床相关TEAE发生率为37.3%,BQT组则为53.2%。大部分TEAE的严重程度为轻度至中度,且未报告与利福特尼唑相关的SAE。这些研究结果显示,与BQT相比,RTT的安全性与耐受性较佳。此外,RTT无需提前进行药敏试验,这一特点凸显其成为标准化一线疗法的潜力,可实现与尿素呼气试验(“UBT”)的无缝衔接。此外,RTT给药更为便捷,再加上更优的安全性和耐受性特征,预计将显著提高患者依从性。
丹诺医药正在为利福特尼唑实施明确的临床开发及商业化策略。通过与远大生命科学签订的独家商业合作协议,公司将借助其强大的营销能力和丰富的商业化资源,支持用于治疗幽门螺杆菌感染的利福特尼唑在中国成功上市。凭借美国食品药物管理局(“FDA”)授予的IND许可、快速通道及合格抗感染产品(“QIDP”)认定,利福特尼唑可能受益于FDA的加速审评流程,有望加快在美国及其他海外市场的上市步伐。除幽门螺杆菌感染外,利福特尼唑在更广泛的抗菌应用领域展现潜力。基于已获得国家药品监督管理局的IND批准,公司计划推进利福特尼唑治疗细菌性阴道病及艰难梭菌感染的临床开发。
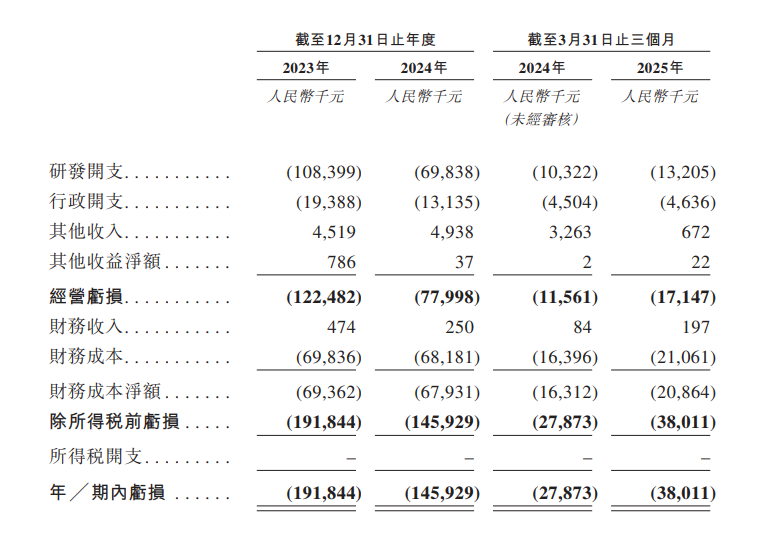
财务方面,于2023年度、2024年度、2024年以及2025年截至3月31日止三个月,丹诺医药经营亏损分别为约1.22亿元、7799.8万元、1156.1万元、1714.7万元人民币;年/期内亏损分别为约1.92亿元、约1.46亿元、2787.3万元、3801.1万元人民币。